Biomarqueurs en oncologie thoracique : recommandations et perspectives
© Edimark – Correspondances en Onco-Théranostic, Vol XIII – n° 4
Points forts
- La détermination du statut PD-L1 et la recherche de multiples altérations oncogéniques (mutations, fusions) par NGS sont recommandées dans les CBNPC non épidermoïdes métastatiques.
- La recherche d’altérations génétiques spécifiques (mutations EGFR, statut ALK) et la détermination du statut PD-L1 sont nécessaires dès le stade localisé résécable des CBNPC non épidermoïdes.
- La recherche des altérations oncogéniques doit également être réalisée dans les carcinomes épidermoïdes des patients non fumeurs ou petits fumeurs.
- La recherche des altérations oncogéniques peut être réalisée sur des prélèvements tissulaires ou cellulaires fixés, sur des liquides biologiques à l’état frais ou à partir de sang prélevé dans des conditions adéquates.
- Les analyses de l’ADN tumoral circulant aux stades précoces et pour la détection de la maladie résiduelle nécessitent des techniques spécifiques ultrasensibles, et leur impact dans la prise en charge thérapeutique reste à évaluer.
Les stratégies thérapeutiques des cancers bronchopulmonaires non à petites cellules (CBNPC) ont été révolutionnées ces dernières années par l’utilisation des thérapies dites « ciblées », et de l’immunothérapie seule ou combinée à la chimiothérapie. Initialement développées dans le contexte de la maladie métastatique, ces stratégies se déclinent désormais aux stades les plus précoces de la maladie, dans le contexte périopératoire. Des tests sont ainsi recommandés aux différents stades de la maladie par le groupe de travail collégial piloté par l’Institut national du cancer (INCa) et la Société européenne d’oncologie médicale (ESMO), fondés sur les médicaments actuellement disponibles en France. Nous envisagerons les évolutions attendues en fonction des essais cliniques récents et détaillerons la place que pourrait prendre l’analyse de l’ADN tumoral circulant dans les prochaines années.
Mots-clés : Biomarqueur – CBNPC – Stade localisé – Recommandations – ADN tumoral circulant.
Recommandations (INCa, ESMO) et leur évolution
Les recommandations publiées par l’INCa concernant les tests moléculaires nécessaires à la prise en charge des patients atteints d’un CBNPC 1, et celles de l’ESMO concernant le diagnostic et la prise en charge clinique des CBNPC avec addiction oncogénique 2 datent du début de l’année 2023. Une révision des recommandations publiées par l’INCa est en cours, et le groupe de travail pour la médecine de précision de l’ESMO a actualisé les indications concernant le séquençage dit « de nouvelle génération » (NGS, next-generation sequencing) pour tous les cancers, dont les CBNPC 3. Les analyses moléculaires sont à réaliser dans tous les sous-types histologiques de CBNPC non épidermoïdes (adénocarcinomes, carcinomes NOS (not otherwise specified), carcinomes neuroendocrines à grandes cellules, carcinomes adénosquameux, carcinomes sarcomatoïdes). Elles sont également recommandées dans le cas des carcinomes épidermoïdes survenant chez le sujet jeune (< 50 ans), petit fumeur (< 15 paquets-année) ou non fumeur (< 100 cigarettes au cours de la vie) ou tabagique sevré depuis plus de 15 ans.
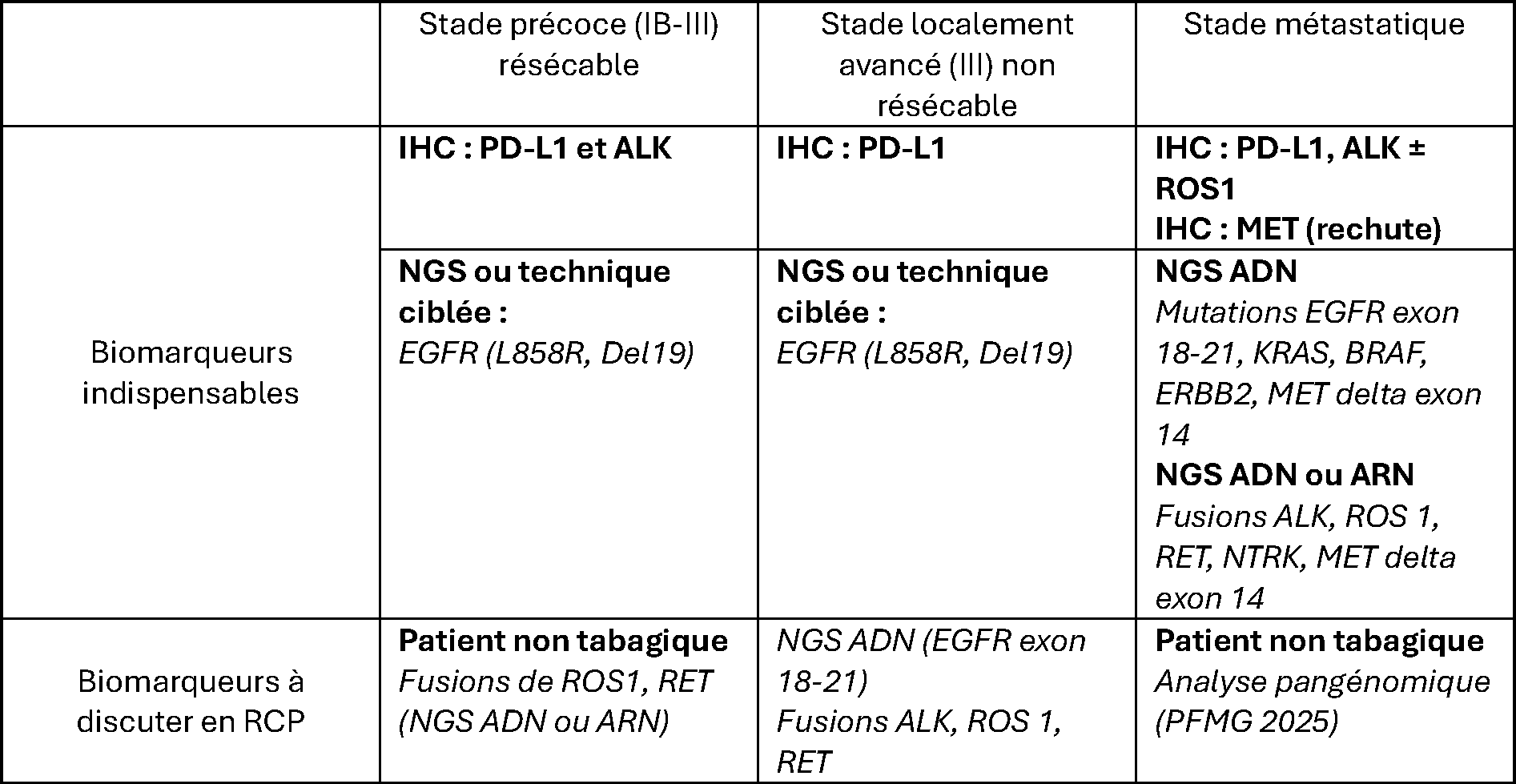
[Tableau 1]
Biomarqueurs à tester dans les CBNPC non épidermoïdes (toute histologie confondues) et épidermoïdes (non fumeur/petit fumeur/ancien fumeur)
IHC : immunohistochimie ; NGS : next-generation-sequencing ; PD-L1 : programmed death-ligand ; PFMG : Plan France médecine génomique
Stades localisés
Au stade de CBNPC localisé opérable, de stade IB-III (selon la 8e édition de la TNM (classification of malignant tumors)), il est nécessaire d’établir sur la biopsie diagnostique le statut PD-L1 et les statuts EGFR et ALK. L’analyse de l’expression de PD-L1 par les cellules tumorales doit se faire selon les critères spécifiés par le groupe des pathologistes français pour le choix des anticorps et être exprimée selon le pourcentage de cellules tumorales marquées (TPS, tumoral proportion score) 4. La recherche des mutations de l’EGFR, au minimum la présence des mutations communes que sont les délétions en phase de l’exon 19 et la mutation faux-sens L858R sur l’exon 21, peut se faire grâce à des techniques de biologie moléculaire ciblées ou par séquençage nouvelle génération. L’analyse du statut ALK sera réalisée le plus souvent en immunohistochimie, avec confirmation par une technique de FISH (fluorescence in situ hybridization) ou en biologie moléculaire dans les cas faiblement positifs (1+ ou 2+).
En fonction de ces résultats et du risque de récidive, il pourra éventuellement être proposé un traitement néoadjuvant par chimio-immunothérapie (stade IIA à IIIB, PD-L1 TPS ≥ 1 %, statuts EGFR et ALK négatifs) ou un traitement adjuvant par anti-EGFR (stade IB à IIIA, présence d’une mutation commune de l’EGFR). Des essais cliniques de phase III ont montré un bénéfice de traitements adjuvants par inhibiteurs de ALK dans les cas de tumeurs ayant un réarrangement de ALK. De plus, des essais de traitement adjuvant ciblant les réarrangements de RET sont en cours.
Stades localement avancés non résécables
Au stade d’un CBNPC localement avancé non résécable, avec indication de radiochimiothérapie, il est nécessaire d’établir le statut PD-L1 et le statut EGFR. Une immunothérapie de consolidation pourra être proposée selon le niveau d’expression de PD-L1 et si la tumeur n’est pas mutée sur le gène EGFR. Le groupe de travail de l’INCa recommande ainsi un séquençage des exons 18-21 de l’EGFR dans cette situation afin d’éviter une immunothérapie chez les patients ayant une addiction oncogénique. Il semblerait raisonnable d’élargir la recherche de biomarqueurs dès ce stade afin d’identifier les autres situations de dépendance oncogénique (notamment les fusions des gènes ALK, ROS1 et RET) qui ne bénéficient pas, ou peu, d’une immunothérapie 5. Cependant, il n’existe pas, à ce jour, de recommandations nationales ou internationales en ce sens.
Stades métastatiques
Au diagnostic d’un CBNPC métastatique, la détermination du statut PD-L1 en immunohistochimie ainsi qu’une analyse large des biomarqueurs avec impact théranostique sont indiquées (tableau 1 et tableau 2) 6. En effet, la 1re ligne de traitement sera conditionnée par la présence d’une mutation EGFR, d’un réarrangement de ALK, ROS1 ou RET. D’autres altérations oncogéniques, comme la mutation BRAF V600E, la mutation KRAS G12C, les mutations conduisant à un saut d’exon 14 de MET ou les fusions de NTRK1/2/3, pourront ouvrir à la prescription d’un traitement ciblé validé par la HAS dès la 2e ligne de traitement. Enfin, la présence d’une mutation ERBB2/HER2 ou d’une fusion NRG1 permettra l’inclusion du patient dans un essai spécifique. Les techniques de séquençage à haut débit permettent de rechercher l’ensemble des cibles validées dès la 1re ligne de traitement : tous les types de mutations EGFR des exons 18-21 (mutations communes, récurrentes non communes, insertions exon 20 et mutations rares) et les fusions des gènes ALK et RET. De plus, elles permettent, à partir du même matériel, et pour un coût réactif identique, d’inclure dans la même analyse, l’ensemble des cibles pertinentes pour les lignes ultérieures de traitement. L’utilisation de techniques de séquençage basées sur l’ARN a montré une meilleure sensibilité que le séquençage de l’ADN pour la détection des transcrits de fusion 7 ou des sauts d’exon 14 de MET. Ces techniques sont donc souvent utilisées en complément des techniques de séquençage à partir d’ADN pour obtenir un profil moléculaire complet des CBNPC. Les techniques ciblées, permettant de rechercher une liste limitée d’altérations génétiques dans un ou plusieurs gènes (notamment EGFR), gardent éventuellement une place dans la pratique pour répondre aux situations d’urgence, sous réserve de ne pas épuiser le matériel et d’être complétées par une analyse NGS si elles sont négatives 8. Les stratégies séquentielles sont à déconseiller, car elles sont source de délais supplémentaires, d’épuisement du matériel et, dans l’ensemble, plus coûteuses 9. Ces analyses moléculaires devront être réalisées en priorité sur le matériel cytologique ou histologique disponible. L’analyse de l’ADN tumoral circulant peut également permettre la recherche d’une altération oncogénique ciblable mais elle nécessite une fraction d’ADN tumoral en circulation suffisante et des techniques adaptées (voir ci-dessous). Elle est recommandée lorsque le matériel cytologique ou histologique initial est en quantité insuffisante pour réaliser les analyses moléculaires et/ou pour optimiser le délai de prise en charge si nécessaire 10.
Maladie en progression
Lors de la progression de la maladie, de nouvelles analyses immunohistochimiques et moléculaires sont indiquées. Chez les patients sans mutation EGFR, l’expression de MET sera analysée en immunohistochimie pour un éventuel traitement par anticorps conjugué à un cytotoxique si la tumeur présente une forte expression membranaire de MET dans plus de 25 % des cellules tumorales ou une amplification du gène.
Pour les patients recevant une thérapie ciblée anti-EGFR ou anti-ALK, il sera nécessaire d’analyser une lésion en progression pour rechercher une transformation histologique en carcinome épidermoïde ou carcinome à petites cellules. Il sera également nécessaire de réaliser un séquençage ADN et/ou ARN pour identifier un mécanisme moléculaire de résistance pouvant conduire à une prise en charge spécifique :
- amplification génique ou mutations secondaires de résistance sur l’oncogène impliqué
- activation de voies de signalisation parallèles (amplification des gènes MET ou ERBB2, réarrangement d’un autre oncogène, mutation du gène BRAF, etc.).
Carcinomes neuroendocrines à grandes cellules
Dans les carcinomes neuroendocrines à grandes cellules, les analyses moléculaires permettent de distinguer les tumeurs qui ont un profil de type adénocarcinome (gènes mutés KRAS, KEAP1 ou STK11) et celles ayant un profil de type carcinome à petites cellules (mutation TP53 et délétion ou mutation de RB1), permettant ainsi d’adapter la chimiothérapie 11. Dans les tumeurs ayant un profil « adénocarcinome », de rares cas de dépendance oncogénique ciblable ont été observés 12.
Analyse complète génomique tumorale
Le Plan France médecine génomique 2025 (PFMG 2025) comporte une indication pour les tumeurs rares ou les tumeurs en échec thérapeutique. Si l’indication est retenue lors d’une réunion de concertation pluridisciplinaire du PFGM 2025, un séquençage du génome tumoral complet, de l’exome et du transcriptome tumoral, à partir d’un prélèvement congelé, pourra être réalisé après consultation d’oncogénétique et consentement signé du patient (https://pfmg2025.aviesan.fr/). Cette analyse est recommandée chez les patients jeunes ou non fumeurs, atteints d’un CBNPC métastatique et pour lesquels il n’a pas été identifié d’altération oncogénique dite « driver mutuellement exclusive » avec les techniques et les panels standard (correspondant à la liste des altérations indiquées dans le (tableau 2), auxquelles il faut associer toutes les mutations oncogéniques de KRAS, y compris celles qui ne sont pas ciblables actuellement). Ces analyses pangénomiques pourront éventuellement révéler un mécanisme oncogénique rare (fusion impliquant une kinase), une amplification ou une délétion génique potentiellement ciblable ou encore une anomalie des systèmes de détection et de réparation des dommages à l’ADN, révélant une susceptibilité particulière de la tumeur à certaines molécules.
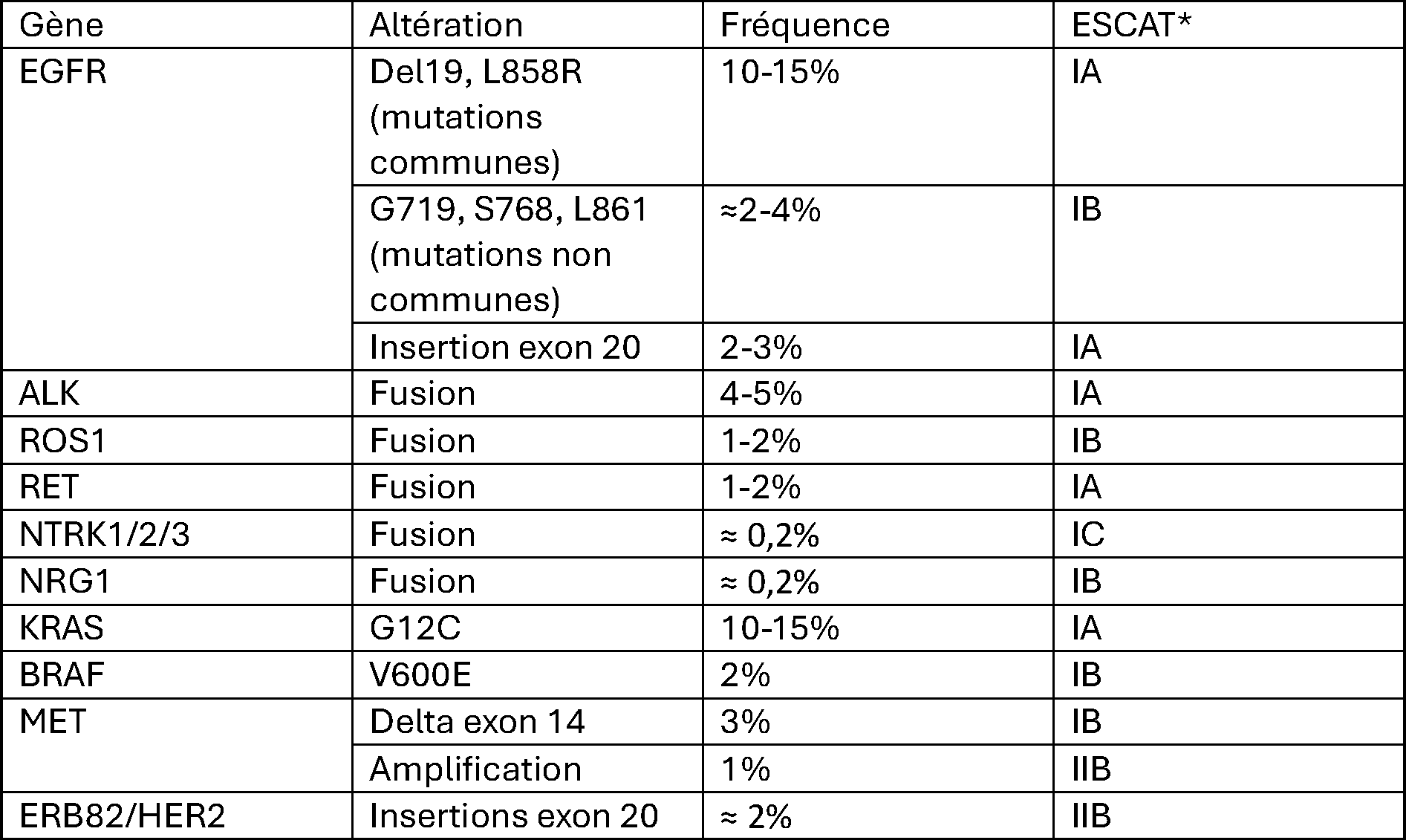
[Tableau 2]
Altérations oncogéniques ciblables dans les CBNPC non épidermoïdes au stade métastatique.
*Classification indiquée selon le groupe de travail sur la médecine de précision de l’ESMO 3
ESCAT : ESMO Scale of clinical actionability of molecular targets10 ; I : altération validée pour une utilisation clinique (bénéfice clinique démontré dans un essai clinique prospectif randomisé IA, prospectif non randomisé IB, essai « basket » IC) ; II : altération en cours d’investigation (étendue du bénéfice clinique inconnue : bénéfice évalué dans une étude rétrospective IIA, dans une étude prospective, mais sans données de survie, IIB).
Analyses sur ADN tumoral circulant
Généralités et aspects méthodologiques
La fraction d’ADN tumoral provenant des cellules tumorales (ADNtc, ADN tumoral circulant) dans l’ADN libre plasmatique (ccfDNA, circulating cell free DNA) est très variable et, le plus souvent, très faible. Dans les CBNPC, cette fraction dépend de l’histologie tumorale (fraction d’ADNtc plus importante dans les carcinomes épidermoïdes que dans les adénocarcinomes), du volume tumoral (fraction d’ADNtc d’environ 0,1 % pour un volume de 10 cm3) et de différents paramètres histologiques (prolifération, nécrose, envahissement vasculaire) 13. Il a aussi été largement démontré que la localisation de la tumeur conditionne le passage d’ADN tumoral dans la circulation (transfert élevé dans les localisations hépatiques mais très limité dans les localisations cérébrales, par exemple). Les conditions pré-analytiques de prélèvement sanguin peuvent également influencer la mesure de la fraction d’ADNtc, puisqu’il y a une lyse leucocytaire avec relargage d’ADN dans le plasma si le sang est prélevé sur EDTA et conservé plusieurs heures avant isolement du plasma, avec le risque de « diluer » la fraction mutée d’intérêt. Il faut comprendre que la quantité d’ADN qui peut être extraite du plasma est limitante pour détecter des anomalies qui ne seront représentées qu’à un taux très faible. En effet, on estime que la quantité d’ADN libre plasmatique (ccfDNA) moyenne est d’environ 5 ng/mL de plasma, et qu’il faut « tester » 20 ng d’ADN (soit environ 6 000 copies) pour détecter de manière fiable et reproductible 0,5 % de fraction mutée (soit 30 copies) sur une position spécifique. Il est donc nécessaire d’utiliser des techniques adaptées en fonction de la situation clinique et, notamment, des techniques ultrasensibles dans le cadre du dépistage au stade précoce ou de la détection de la maladie résiduelle postopératoire. Pour le dépistage, les techniques sont par définition « agnostiques », les plus sensibles étant fondées sur l’analyse de la fragmentation de l’ADN ou l’analyse du profil de méthylation, tandis que d’autres combinent la recherche de variants ponctuels et des analyses protéomiques14. Pour le suivi de la maladie résiduelle, les techniques les plus sensibles reposent sur la recherche d’un très grand nombre de variants préalablement identifiés dans la tumeur (technique dite tumor informed) 15.
Pour la recherche d’une cible théranostique au stade métastatique, la plupart des solutions commerciales ont la capacité de détecter des variations ponctuelles (SNV/indel, single nucleotide variant/insertion-deletion) et des réarrangements géniques représentés à une fraction de 0,2-1 % en fonction de la quantité totale d’ADN testé (10-50 ng). La recherche de transcrits de fusion nécessite des techniques de séquençage NGS fondées sur la capture de régions cibles, car :
- les cassures et les réarrangements géniques surviennent au niveau des régions introniques qui sont généralement de grande taille ;
- il n’y a pas, actuellement en routine, de technique fondée sur l’analyse de l’ARN circulant.
La détection d’une amplification génique nécessite une fraction d’ADN tumorale suffisante (évaluée à > 20 % dans le cas de certains kits).
Stades précoces : aide au staging et détection de la maladie résiduelle
L’étude TRACERx, coordonnée par Charles Swanton (NCT01888601), a largement contribué à l’analyse de l’évolution clonale et de la dissémination tumorale dans les stades précoces des cancers du poumon. Dans l’étude publiée par Chris Abbosh en 2023, l’analyse de l’ADNtc, fondée sur la recherche spécifique de 200 variants préalablement identifiés dans la tumeur, a atteint une sensibilité de détection de fraction mutée de 0,01 % (correspondant approximativement à un volume tumoral de 1 cm3). L’analyse réalisée rétrospectivement sur le plasma collecté en préopératoire indique que la positivité du test est corrélée à la survie globale et au restaging pathologique des patients évalués cN0/N1 en atteinte pN2 dans les adénocarcinomes. La positivité du test, lors de l’analyse de la maladie résiduelle dans les 4 mois postopératoires, est associée à des rechutes plus précoces, notamment extrathoraciques 16. Des résultats similaires sont rapportés dans d’autres publications. Compte tenu du développement actuel des stratégies thérapeutiques périopératoires, ces tests auraient le potentiel d’affiner le staging préopératoire et de guider l’intensification ou au contraire la désescalade des traitements ciblés ou des chimio-immunothérapies périopératoires, s’ils font la preuve de leur utilité clinique. L’utilisation de ce « nouveau » biomarqueur dans le contexte des stades précoces dépendra des résultats des études interventionnelles en cours ou à venir et nécessitera l’accès à des tests ultrasensibles, indispensables dans ce contexte 15.
Conclusion
Le CBNPC non épidermoïde constitue un modèle dans le domaine des biomarqueurs. Il est caractérisé par de multiples altérations oncogéniques pour lesquelles il existe des thérapies ciblées efficaces. La recherche de ces altérations nécessite aujourd’hui la mise en œuvre en routine d’un séquençage NGS à partir d’ADN et/ou ARN, sur cellules ou tissus fixés ou sur liquides biologiques, avant l’instauration de la 1re ligne de traitement en situation métastatique. La place de ces techniques d’analyse moléculaire en routine est reconnue et validée par l’INCa, la HAS 17 et l’ESMO. Malgré la place incontournable de l’immunothérapie dans cette pathologie, le seul biomarqueur qui ait fait la preuve de son utilité en routine clinique reste la détermination du statut PD-L1 en immunohistochimie 18. La connaissance de ces altérations moléculaires a également conduit à personnaliser la prise en charge des stades précoces. Les prochaines avancées attendues concernent une meilleure individualisation des stratégies périopératoires en fonction de l’analyse de l’ADNtc, marqueur de dissémination et d’agressivité de la maladie.
(1) INCa. Patients atteints d’un cancer bronchique non à petites cellules : indications des tests moléculaires en vue de la prescription de traitements de précision. 2023. https://www.e-cancer.fr/Expertises-et-publications/Catalogue-des-publications/Patients-atteints-d-un-cancer-bronchique-non-a-petites-cellules-indications-des-tests-moleculaires-en-vue-de-la-prescription-de-traitements-de-precision
(2) Hendriks LE et al. Oncogene-addicted metastatic non-small-cell lung cancer: ESMO clinical practice guideline for diagnosis, treatment and follow-up. Ann Oncol 2023;34(4):339-57.
(3) Mosele MF et al. Recommendations for the use of next-generation sequencing (NGS) for patients with advanced cancer in 2024: a report from the ESMO Precision Medicine Working Group. Ann Oncol 2024;35(7):588-606.
(4) Adam J et al. Multicenter harmonization study for PD-L1 IHC testing in non-small-cell lung cancer. Ann Oncol 2018;29(4):953-8.
(5) Mazieres J et al. Immune checkpoint inhibitors for patients with advanced lung cancer and oncogenic driver alterations: results from the IMMUNOTARGET registry. Ann Oncol 2019;30(8):1321-8.
(6) Mateo J et al. A framework to rank genomic alterations as targets for cancer precision medicine: the ESMO scale for clinical actionability of molecular targets (ESCAT). Ann Oncol 2018;29(9):1895-902.
(7) Benayed R et al. High yield of RNA sequencing for targetable kinase fusions in lung adenocarcinomas with no mitogenic driver alteration detected by DNA sequencing and low tumor mutation burden. Clin Cancer Res 2019;25(15):4712-22.
(8) Khalifa E et al. Idylla EGFR assay on extracted DNA: advantages, limits and place in molecular screening according to the latest guidelines for non-small-cell lung cancer (NSCLC) patients. J Clin Pathol 2023;76(10):698-704.
(9) Zou D et al. Diagnostic value and cost-effectiveness of next-generation sequencing-based testing for treatment of patients with advanced/metastatic non-squamous non-small-cell lung cancer in the united states. J Mol Diagn 2022;24(8):901-14.
(10) Rolfo C et al. Liquid biopsy for advanced NSCLC: a consensus statement from the International Association for the Study of Lung Cancer. J Thorac Oncol 2021;16(10):1647-62.
(11) Rekhtman N et al. Next-generation sequencing of pulmonary large cell neuroendocrine carcinoma reveals small cell carcinoma-like and non-small cell carcinoma-like subsets. Clin Cancer Res 2016;22(14):3618-29.
(12) Ferrara MG et al. Large cell neuro-endocrine carcinoma of the lung: current treatment options and potential future opportunities. Front Oncol 2021;11:650293.
(13) Abbosh C et al. Phylogenetic ctDNA analysis depicts early-stage lung cancer evolution. Nature 2017;545(7655):446-51.
(14) Rolfo C, Russo A. Brave new world of cfDNA-omics for early cancer detection. J Immunother Cancer 2023;11(9):e006309.
(15) Abbosh C et al. Implementing circulating tumor DNA as a prognostic biomarker in resectable non-small cell lung cancer. Trends Cancer 2024;10(7):643-54.
(16) Abbosh C et al. Tracking early lung cancer metastatic dissemination in TRACERx using ctDNA. Nature 2023;616(7957):553-62.
(17) HAS. Séquençage haut débit ciblé d’un panel de gènes dans la prise en charge médicale du cancer du poumon : recherche des altérations moléculaires somatiques. 2024. https://www.has-sante.fr/jcms/p_3535386/fr/sequencage-haut-debit-cible-d-un-panel-de-genes-dans-la-prise-en-charge-medicale-du-cancer-du-poumon-recherche-des-alterations-moleculaires-somatiques
(18) Sholl LM et al. Programmed death Ligand-1 and tumor mutation burden testing of patients with lung cancer for selection of immune checkpoint inhibitor therapies: guideline from the College of American Pathologists, Association for Molecular Pathology, International Association for the Study of Lung Cancer, Pulmonary Pathology Society, and LUNGevity Foundation. Arch Pathol Lab Med 2024;148(7):757-74.